Sr. Director:
He leído con interés el caso clínico publicado en su revista diagnosticado de síndrome de activación macrofágica (SAM) y artritis juvenil de comienzo sistémico (AJS)1, del que quisiera hacer varias consideraciones.
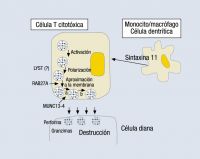
 Como comentan los propios autores, el SAM presenta características clínicas similares a la linfohistiocitosis hemofagocítica (LHH) y, de hecho, no debería considerarse fuera de dicha entidad2, como recomienda la propia Sociedad Histiocitaria3 y alguno de los autores citados en el artículo4. La LHH es un cuadro grave que puede ser de origen genético (familiar) o adquirido desencadenado por infecciones, procesos malignos, algunas metabolopatías y también por enfermedades autoinmunitarias o reumatológicas (el llamado SAM)3-6. Los criterios diagnósticos propuestos por la Sociedad Histiocitaria para la LHH3 se muestran en la tabla 1. La patogenia común es la presencia de un defecto adquirido o congénito de la función NK y citotóxica, que impide la destrucción de la célula infectada manteniéndose la actividad inflamatoria de las células histiocitarias y linfocitos T con persistencia de niveles altos de citocinas, que son las que originan el cuadro clínico5,6. Tanto las formas familiares como las adquiridas pueden estar desencadenadas por infecciones, y las más frecuentes son las producidas por virus del tipo herpes, como el virus de Ebstein-Barr o el de la varicela6, como en el caso publicado1. Por ello, es difícil diferenciar ambos cuadros si no hay antecedentes familiares, ya que son clínica y anatomopatológicamente indistinguibles3,5, y debe sospecharse la posibilidad de un origen genético cuando la enfermedad se manifiesta en el primer año de vida5. El descubrimiento de mutaciones en varios genes implicados ha demostrado que también hay casos familiares que se manifiestan tardíamente, hasta la cuarta década de la vida5,6. Los genes descritos afectan al gen de la perforina (PRF1), al MUNC13-4 (o UNC13D), a la sintaxina 11 (STX11) y, al menos, a otro gen desconocido localizado en el cromosoma 93,5. Todos ellos, junto con los genes afectados en la enfermedad de Griscelli, en la enfermedad de Chediag-Higashi o en el síndrome linfoproliferativo ligado al cromosoma X, afectan a la capacidad de liberación y el tráfico de gránulos citolíticos desde la célula efectora a la célula diana5, como se muestra en la figura 1.
Como comentan los propios autores, el SAM presenta características clínicas similares a la linfohistiocitosis hemofagocítica (LHH) y, de hecho, no debería considerarse fuera de dicha entidad2, como recomienda la propia Sociedad Histiocitaria3 y alguno de los autores citados en el artículo4. La LHH es un cuadro grave que puede ser de origen genético (familiar) o adquirido desencadenado por infecciones, procesos malignos, algunas metabolopatías y también por enfermedades autoinmunitarias o reumatológicas (el llamado SAM)3-6. Los criterios diagnósticos propuestos por la Sociedad Histiocitaria para la LHH3 se muestran en la tabla 1. La patogenia común es la presencia de un defecto adquirido o congénito de la función NK y citotóxica, que impide la destrucción de la célula infectada manteniéndose la actividad inflamatoria de las células histiocitarias y linfocitos T con persistencia de niveles altos de citocinas, que son las que originan el cuadro clínico5,6. Tanto las formas familiares como las adquiridas pueden estar desencadenadas por infecciones, y las más frecuentes son las producidas por virus del tipo herpes, como el virus de Ebstein-Barr o el de la varicela6, como en el caso publicado1. Por ello, es difícil diferenciar ambos cuadros si no hay antecedentes familiares, ya que son clínica y anatomopatológicamente indistinguibles3,5, y debe sospecharse la posibilidad de un origen genético cuando la enfermedad se manifiesta en el primer año de vida5. El descubrimiento de mutaciones en varios genes implicados ha demostrado que también hay casos familiares que se manifiestan tardíamente, hasta la cuarta década de la vida5,6. Los genes descritos afectan al gen de la perforina (PRF1), al MUNC13-4 (o UNC13D), a la sintaxina 11 (STX11) y, al menos, a otro gen desconocido localizado en el cromosoma 93,5. Todos ellos, junto con los genes afectados en la enfermedad de Griscelli, en la enfermedad de Chediag-Higashi o en el síndrome linfoproliferativo ligado al cromosoma X, afectan a la capacidad de liberación y el tráfico de gránulos citolíticos desde la célula efectora a la célula diana5, como se muestra en la figura 1.
Los casos de SAM aparecen, en general, más tarde, y suelen ser menos graves que los congénitos o que los adquiridos tras infecciones, aunque también pueden ser mortales5,7. En el caso publicado llama la atención que se hizo el diagnóstico de AJS a los 9 meses, por un síndrome febril prolongado con hepatosplenomegalia sin afectación articular, en el que había una elevación de la proteína C reactiva (PCR) y del factor reumatoide. No se descarta que en realidad se tratara de una primera manifestación de LHH, pues desconocemos si había otros parámetros analíticos que lo apoyaran, y el hecho de que en ese primer momento la punción de médula ósea fuera normal no lo descarta, ya que la LHH es un cuadro progresivo y la hemofagocitosis puede no demostrarse al principio5,6. Los corticoides actúan como linfocidas e inhiben la expresión de citocinas y quimiocinas5, que pueden haber abortado el cuadro inicial, siendo insuficiente para la curación del mismo, sobre todo si, por la precocidad de la aparición de la clínica, se trata de un caso familiar. Es interesante el hecho de que 4 días después del comienzo de la fiebre por la varicela presentara esplenomegalia en la exploración, un dato absolutamente atípico en una varicela no complicada. La sospecha diagnóstica de LHH debe ser precoz, dado que el cuadro puede ser fulminante si no se instaura un tratamiento adecuado, como ocurrió en este caso. La Sociedad Histiocitaria ha elaborado un protocolo de tratamiento3 en el que se emplea dexametasona, ciclosporina y etopósido (disponible en www.histio.org/society/protocols). Presenta pequeñas variaciones frente a uno inicial, que ha demostrado su eficacia tanto en las formas genéticas como en las adquiridas8, incluido el SAM. La remisión completa tras el tratamiento farmacológico sería suficiente para las formas adquiridas, pero la reaparición o la reactivación del cuadro, o el diagnóstico de una forma genética (por historia familiar o diagnóstico genético), necesita además el trasplante de células progenitoras hematopoyéticas para su curación definitiva3,8.
Janka5 reconoce que es difícil diferenciar el SAM de otras formas de LHH cuando falta la artritis, y sugiere que en su experiencia una PCR elevada (como tenía la paciente) apoyaría el primer diagnóstico. Aunque el tratamiento menos agresivo del SAM puede ser eficaz, sobre todo en niños mayores sin un aparente factor desencadenante, como comentan los autores1, en este caso grave, desarrollado tras la varicela, debería haberse empleado el tratamiento propuesto por la Sociedad Histiocitaria si la entidad se hubiera sospechado y diagnosticado antes de su fallecimiento.
Bibliografía
- Aleo Luján E, Gil López C, Balboa de Paz F, Kilmurray GL, Pérez Rodríguez O, Rubial Francisco JL. Síndrome de activación de macrófagos y artritis juvenil de inicio sistémico. Acta Pediatr Esp. 2007; 65: 304-308.
- Remanan AV, Baildam EM. Macrophage activation syndrome is hemophagocytic lymphohistiocytosis-need for the right terminology. J Rheumathol. 2002; 29: 1.105.
- Henter JI, Horne AC, Aricò M, Egeler RM, Filipovich AH, Imashuku S, et al. HLH-2004: diagnostic and therapeutic guidelines for hemophagocytic lymphohistiocytosis. Pediatr Blood Cancer. 2007; 48: 124-131.
- Ravelli A. Macrophage activation syndrome. Curr Opin Rheumatol. 2002; 14: 548-552.
- Janka GE. Familial and acquired hemophagocytic lymphohistiocytosis. Eur J Pediatr. 2007; 166: 95-109.
- Filipovich AH. Hemophagocytic lymphohistiocytosis and related disorders. Curr Opin Allergy Clin Immunol. 2006; 6: 410-415.
- Chen HH, Kuo HC, Wang L, Yu H, Shen JM, Kwang KP, et al. Childhood macrophage activation syndrome differs from infection-associated hemophagocytosis syndrome in etiology and outcome in Taiwan. J Microbiol Immunol Infect. 2007; 40: 265-271.
- Henter IH, Samuelsson-Horne AC, Aricò M, Egeler RM, Elinder G, Filipovich AH, et al. Treatment of hemophagocytic lymphohistiocytosis with HLH-94 immunochemotherapy and bone marrow transplantation. Blood. 2002; 100: 2.367-2.373.














